displazia Fibromuscular (FMD) este un idiopatică, noninflammatory, nonatherosclerotic boli vasculare de dimensiuni mici și mijlocii artere.1,2 deoarece a fost identificat pentru prima dată în 1938, FMD a fost descris în aproape fiecare pat arterial, dar cel mai frecvent afectează arterele carotide renale și extracraniene. Acest articol se concentrează asupra FMD cerebrovasculare, simptome neurologice comune asociate cu FMD și relația dintre FMD și accident vascular cerebral.,deoarece FMD este frecvent identificat la persoanele asimptomatice, identificarea prevalenței exacte și a istoricului natural este dificilă. Conform Registrului FMD din SUA, vârsta medie la diagnostic este de 51,9, 90% dintre persoanele diagnosticate cu FMD sunt femei, 72% au hipertensiune arterială și 60% au dureri de cap semnificative.3 o minoritate de persoane cu FMD raportează o rudă apropiată cu FMD, deși aproximativ 80% dintre rudele de gradul I sau ii au hipertensiune arterială și 53, 5% raportează antecedente de accident vascular cerebral., Este la fel de frecvent ca FMD să afecteze arterele renale și cerebrocervicale, cu aproximativ o coprevalență de 65%.3 angiografia CT modernă (CTA) și angiografia prin rezonanță magnetică cu contrast îmbunătățit (MRA) au îmbunătățit caracterizarea radiografică și diagnosticul FMD. Dintre persoanele cu FMD cerebrocervical, 95% au implicare carotidă, adesea bilaterală, iar 70% au implicare a arterelor vertebrale.,Fiziopatologia FMD este puțin înțeleasă, deși dovezile histologice sugerează o transformare defectuoasă a fibroblastelor celulelor musculare netede duce la degradarea laminelor elastice, a sintezei aberante de colagen și a fibroplaziei segmentale.5 adulții au cel mai frecvent fibroplazie mediană, mai degrabă decât alte subtipuri histologice.4,6 dovezi puternice susțin heritabilitatea FMD cu o coprevalență ridicată a FMD la gemeni și rude de gradul întâi, deși nu există forme cunoscute cu o singură genă.,4 Recenta asociere la nivelul întregului genom studii au identificat prima gena locus asociate cu febră aftoasă, polimorfismul unei singure nucleotide (rs9349379) în fosfatazei și actina reglementare 1 genă (PHACTR1) pe cromozomul 6.7 Această variantă este, de asemenea, asociate cu migrena, disecție de arteră cervicală (Adar), și spontane ruptură a arterei coronare, și este invers asociat cu ateromatoase coronariene și calcifiere.8 varianta PHACTR1 este cunoscută pentru a regla expresia endotelinei-1, un vasoconstrictor endogen.,9
prezentare și diagnostic
prezentarea clinică a FMD depinde de patul vascular afectat (figura 1). În toate locațiile, 3 cele mai frecvente simptome care prezintă includ hipertensiune arterială, dureri de cap și tinitus pulsatil.3 cel mai frecvent simptom prezent al FMD cerebrocervical este tinitusul pulsatil, adesea descris ca whooshing în ureche. Un bruit carotidian poate fi adesea auscultat la examenul fizic, corelând cu fluxul turbulent în arterele cervicale afectate. La cei afectați de FMD cerebrovascular, 70% au dureri de cap, cu 30% sau mai mult caracterizate ca migrenă., Persoanele cu FMD cerebrocervical pot fi, de asemenea, diagnosticate concomitent cu disecția arterei cervicale, prezentând sau fără atac ischemic tranzitoriu (AIT) sau accident vascular cerebral.
Faceți clic pentru a vizualiza mai mare
Figura 1. Apariția celor mai frecvente semne și simptome de displazie fibromusculară.diagnosticul și clasificarea FMD se bazează pe aspectul angiografic., FMD Multifocal reprezintă 90% din cazuri și se caracterizează printr-un aspect de șir de margele reprezentând dilatarea arterială alternativă și constricția (Figura 2). FMD Focal reprezintă 10% din cazuri și se caracterizează printr-o îngustare uniformă concentrică sau tubulară uniformă,10 cel mai adesea în segmentele medii și distale ale arterei carotide interne și segmentul V3-V4 al arterelor vertebrale. FMD intracraniană este rară și mai răspândită la copiii cu subtipuri FMD intimale.5 nu este necesară nicio modalitate imagistică specială pentru diagnosticare, dar CTA sau MRA sunt utilizate cel mai frecvent.,10 arteriografia de scădere digitală (DSA) este imagistica standard pentru diagnostic, dar este mai invazivă, în special pentru persoanele cu FMD care pot prezenta un risc mai mare de disecție iatrogenică. Ultrasonografia Duplex poate fi utilă pentru diagnosticarea și monitorizarea FMD carotide. Cu toate acestea, FMD există adesea în segmentul mijlociu sau distal al arterelor carotide, iar ultrasunetele sunt mai puțin sensibile pentru evaluarea arterelor vertebrale cervicale.
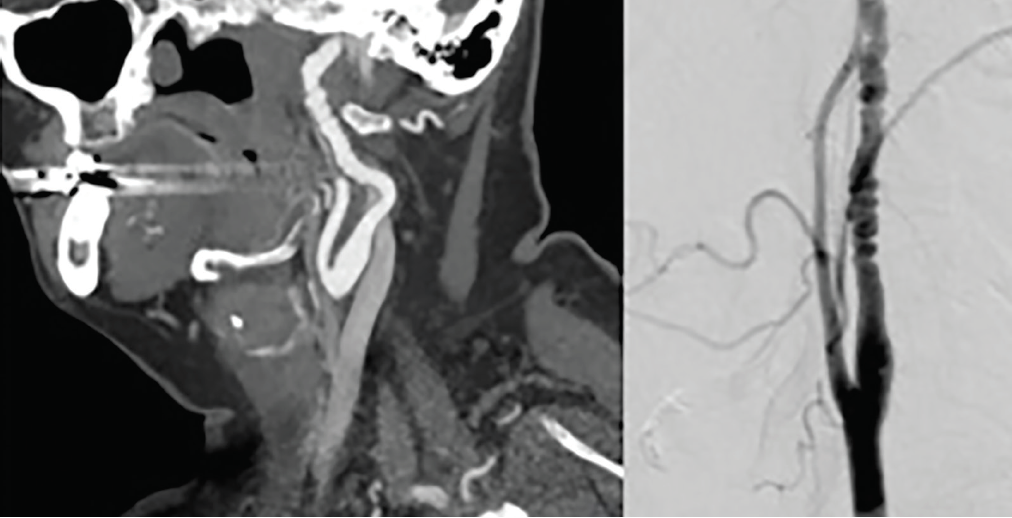
Faceți clic pentru a vedea mai mare
Figura 2., Artera Carotidă Displazie Fibromusculară. O angiografie (stânga) și scădere digitale angiografie (dreapta) demonstratebeading aspectul alternativ cu stenoze și dilatare în concordanță cu displazia fibromuscular (FMD) în midcervical de artera carotidă internă.manifestări neurologice istoricul natural observat al FMD în cazurile asimptomatice diagnosticate întâmplător este relativ benign.,1 Cu toate acestea, în unele cazuri, diagnosticul inițial al FMD se face în stabilirea accidentului vascular cerebral, care, ca manifestare a FMD, este cel mai adesea din cauza disecției concomitente a arterei cervicale (CeAD). În comparație cu populația generală, FMD este asociată cu o prevalență mai mare a anevrismelor intracraniene, în special la femei. În registrul FMD din SUA, peste 40% dintre persoanele cu FMD raportează cu CeAD sau anevrism asociat, deși acest lucru este probabil o supraestimare a adevăratei istorii naturale date de sesizare și eșantionare părtinire în această populație.11
Migrene Dureri de cap., Cea mai frecventă manifestare neurologică a FMD este migrena. Aproape 80% dintre persoanele cu FMD cerebrocervical raportează dureri de cap, cel mai frecvent migrenă.12,13 relația dintre cefaleea și FMD este puțin înțeleasă și probabil multifactorială. Mecanismele propuse includ fluxul sanguin cerebrovascular nonlaminar, hipertensiunea necontrolată, dereglarea reglării simpatice în peretele arterei cervicale sau sensibilitatea crescută la durerea durală. Migrena refractară se poate manifesta, de asemenea, ca simptom prezent sau sechelă reziduală a CeAD.,13 din punct de vedere clinic, simptomele neurologice tranzitorii în FMD care rezultă din aura migrenei sunt adesea diagnosticate greșit ca AIT și necesită o adjudecare atentă pentru a ghida managementul.
disecția arterei cervicale (CeAD). Definiția CeAD este prezența unui hematom mural în peretele unei artere cervicale (carotide sau vertebrale) care rezultă fie dintr-o ruptură intimă, fie din sângerare directă în perete, secundară unei rupturi vasa vasorum.,14 incidența estimată a CeAD în populația generală este de 2 până la 3 la 100.000, deși incidența reală este probabil mai mare la persoanele cu FMD și alte vasculopatii ale țesutului conjunctiv predispozant.15,16 Coprevalence de CeAD și cerebrocervical FMD variază de la 5% la 15% în studiile observaționale, și este mai mare la cei care prezintă mai multe CeAD.5,10,17 aproximativ 70% din CeAD prezintă accident vascular cerebral sau AIT care poate fi adesea întârziat cu zile sau săptămâni de la disecția arterială inițială., Accident vascular cerebral Ischemic cel mai adesea rezultă din formarea tromboembolică sau ocluzia completă la locul disecției. Rar, o disecție a arterei vertebrale care se extinde în segmentul intradural se poate manifesta ca hemoragie subarahnoidă (SAH).14
În plus, CeAD poate prezenta și alte simptome focale neurologice, inclusiv sindromul Horner parțial (adică ptoza ipsilaterală și mioză) de la întreruperea tracturilor oculosimpatice ascendente în artera carotidă internă. Mai puțin frecvent, paraliziile inferioare ale nervului cranian (CN) apar din ischemia sau leziunea asociată a nervilor glossopharyngeal sau vagus., În contrast, disecția arterei vertebrale prezintă frecvent un sindrom vestibular acut, cu sau fără accident vascular cerebral de circulație posterioară care implică teritoriul arterei cerebeloase inferioare posterioare (PICA) și infarct medular lateral și/sau cerebelos. Este important să recunoaștem că în CeAD, disecțiile carotide sau vertebrale cauzează adesea dureri ipsilaterale ale feței sau gâtului de intensitate moderată și o durere de cap nespecifică care poate imita migrena sau cefaleea cluster.,14 din cauza acestei asocieri, incidența durerii acute la nivelul gâtului sau feței cu orice simptome neurologice focale noi la o persoană cu FMD necesită o evaluare neurologică urgentă și imagistica vasculară cervicală pentru a exclude CeAD.anevrisme intracraniene. În orice loc arterial, FMD este asociat cu o prevalență crescută a anevrismelor intracraniene (IA), în special la femei.,18,19 în Registrul FMD din SUA, 13% dintre femeile care au avut imagistică intracraniană au avut cel puțin 1 IA și 4% au avut mai multe IAs, deși prevalența exactă în populația generală cu FMD este necunoscută din cauza părtinirii eșantionării în datele din registru. Riscul ruperii anevrismului poate fi mai mare la pacienții cu FMD la dimensiuni mai mici, deși acest lucru este controversat. Ca și în populația generală, fumatul este semnificativ asociat cu creșterea IA și formarea la persoanele cu FMD.10,11,18 nu este clar dacă persoanele cu FMD necesită o monitorizare angiografică mai frecventă pentru IAs fără întrerupere.,Managementul FMD cerebrocervical depinde în mare măsură de simptomele prezente și de orice complicații neurologice asociate, cum ar fi CeAD, migrenă sau anevrism. În timp ce orientările bazate pe dovezi lipsesc, o înțelegere atentă a abordării diagnostice a FMD și a istoricului natural așteptat ghidează opinia experților și consilierea adecvată a pacienților cu privire la riscul lor cerebrovascular.Managementul cefaleei la persoanele cu sau fără FMD este similar și în mare măsură determinat de o caracterizare exactă a subtipului de cefalee., Managementul migrenei la cei cu sau fără oglinzi FMD este, de asemenea, similar, luând în considerare atât strategiile preventive, cât și terapia abortivă atunci când este indicat. Cu toate acestea, un aspect important la pacienții cu FMD privește utilizarea medicamentelor avortive vasoactive, cum ar fi ergoturile și triptanii, care pot introduce un risc suplimentar la pacienții deja expuși riscului de accident vascular cerebral sau disecție.18 aceasta este o preocupare deosebită pentru persoanele cu FMD și un istoric concomitent de disecție spontană a arterei coronare (SCAD), la care medicamentele vasoconstrictive, cum ar fi triptanii, sunt contraindicație absolută., Terapiile abortive Alternative pentru migrena acută în stabilirea FMD pot include clasa antidopaminergică (de exemplu, proclorperazină, metoclopramidă) sau o scurtă conicitate a steroizilor. Injecțiile cu toxină botulinică pot fi, de asemenea, eficiente pentru migrena cronică refractară în FMD. Mai recent, aprobarea inhibitorilor peptidei legate de gena calcitoninei (CGRP) oferă încă o strategie posibilă eficientă pentru tratarea migrenei în FMD., Deși studiile clinice care aprobă acești noi agenți nu au evidențiat efecte secundare cardiovasculare sau cerebrovasculare semnificative,sunt necesare 20 de observații longitudinale suplimentare și practici din lumea reală pentru a verifica acest lucru.vârsta mediană pentru incidența CeAD este la începutul anilor 40, deși persoanele cu FMD și alte vasculopatii ale țesutului conjunctiv pot prezenta un risc mai mare la vârste mai tinere. Avc și AIT sunt asociate cu CeAD în aproximativ 70% din cazuri, și apar de obicei în primele câteva săptămâni postdissection., Incidența accidentului vascular cerebral sau AIT este adesea latentă la leziunile arteriale, deoarece hematomul intramural se extinde și riscul de tromboembolism intraluminal crește. Pe măsură ce vasul se vindecă peste săptămâni până la luni, riscul de accident vascular cerebral scade cu un risc estimat de recurență pe termen lung, variind în incidență de la 1% la 3%.21-23
nu există încă studii clinice care să investigheze tratamentul CeAD specific FMD, astfel încât managementul este extrapolat din tratamentul CeAD în general., De CADISS studya față de 3 până la 6 luni de terapie antiplachetară cu 3 până la 6 luni de tratament anticoagulant cu warfarină și-a arătat nici o diferență în recurența avc după ce inițial CeAD eveniment. Acest studiu a dus la o recomandare de clasa IIa, de nivel B, care echivalează antiplachetare și anticoagulare timp de 3 până la 6 luni după ce CeAD.24 cu toate acestea, nu există niciun raport privind numărul de participanți la acest proces care au avut și FMD., De asemenea, nu au existat studii solide care să studieze în mod specific utilizarea anticoagulantelor orale cu acțiune directă (de exemplu, apixaban, rivaroxaban sau dabigatran) ca prevenție secundară timpurie în CeAD și FMD. Cu toate acestea, terapia antiplachetară poate fi preferată datorită siguranței și confortului, cu excepția cazului în care există trombi intraluminali clari sau evenimente tromboembolice recurente, în ciuda terapiei antiplachetare.nu există studii randomizate privind tratamentul endovascular al CeAD în stabilirea FMD., Cu toate acestea, deoarece stenoza vaselor după CeAD se recanalizează de obicei fără a fi nevoie de intervenție, terapia endovasculară trebuie rezervată celor care au hipoperfuzie cerebrală recurentă sau evenimente tromboembolice, în ciuda terapiei antitrombotice optimizate.25 de persoane cu FMD pot prezenta, de asemenea, un risc mai mare de disecție iatrogenică prin intervenții pe bază de cateter și acest lucru trebuie luat în considerare în ceea ce privește riscul periprocedural.,cei cu FMD cu risc de incident sau recurent CeAD sunt sfătuiți să evite activitățile asociate cu hiperextensia extremă sau rotația laterală a gâtului, în special manipularea coloanei vertebrale cervicale Chiropractice. Trebuie să se acorde atenție amortizării gâtului în timpul intervenției chirurgicale, programărilor dentare sau altor activități prelungite cu hiperextensie forțată. Exercițiile de rutină și activitățile cardiovasculare nu reprezintă o contraindicație, cu excepția cazului în care există, de asemenea, un istoric însoțitor de disecție spontană a arterei coronare care necesită moderație suplimentară.,apariția accidentului vascular cerebral ischemic la persoanele cu FMD în absența CeAD asociat sau a altui mecanism tromboembolic rămâne controversată. Cu toate acestea, tratamentul AVC acut la pacienții cu FMD trebuie să respecte recomandările standard privind AVC.26 de exemplu, un diagnostic cunoscut de FMD nu este o contraindicație pentru terapia fibrinolitică sau trombectomia Mecanică în alte cazuri eligibile.,
Oamenii cu FMD și istoric de accident vascular cerebral ar trebui să fie pe antiplachetar medicamente pentru prevenția secundară, dacă nu există o competiție accident vascular cerebral mecanism care justifică anticoagulant cum ar fi fibrilație atrială paroxistică sau o stare de hipercoagulare. În special, statinele nu sunt indicate în primul rând pentru prevenirea accidentului vascular cerebral secundar la persoanele cu CeAD în stabilirea FMD și, într-adevăr, pot avea o relație inversă cu riscul de disecție arterială.27,28
FMD asimptomatic
FMD asimptomatic atunci când este descoperit întâmplător are o istorie naturală favorabilă., Indiferent, declarațiile de consens sugerează imagistica vasculară de 1 dată de la creier la pelvis, fie cu CTA, fie cu MRA, pentru a detecta anevrisme, disecții și FMD în alte paturi arteriale.29 pentru persoanele cu FMD și fără antecedente de accident vascular cerebral, beneficiul pe termen lung al terapiei antiplachetare pentru prevenirea primară a accidentului vascular cerebral nu este cunoscut și trebuie evaluat în comparație cu riscul de sângerare pe termen lung.,o vasculopatie neaterosclerotică rară, neinflamatorie, FMD afectează cel mai frecvent arterele renale și cervicale, este mult mai frecventă la femei și este diagnosticată fie întâmplător pe imagistica vasculară, fie cu simptome de cefalee și tinitus care se prezintă la vârsta medie. Incidența accidentului vascular cerebral în FMD este asociată în primul rând cu CeAD și poate fi gestionată conservator cu terapia antiplachetară și evitarea efortului cervical cu risc ridicat. Pacienții cu FMD trebuie, de asemenea, luați în considerare pentru screeningul și monitorizarea formării și creșterii IA., Sunt necesare cercetări suplimentare (Figura 3) pentru a înțelege mai bine genetica, fiziopatologia și tratamentul optim pentru pacienții simptomatici cu FMD și, sperăm, pentru a evita complicațiile cerebrovasculare care pot fi prevenite.
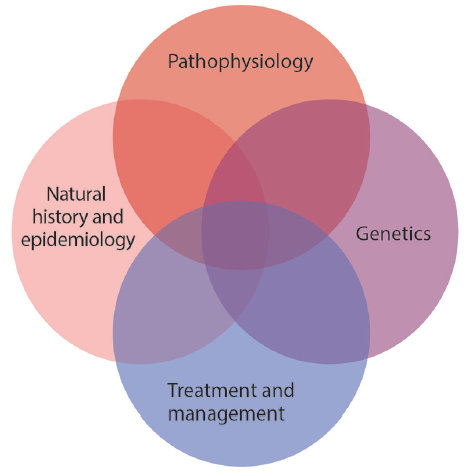
Faceți clic pentru a vedea mai mare
Figura 3. O serie de priorități de cercetare va avansa înțelegerea displazia fibromuscular (FMD), dezvoltarea de terapii și screening-ul și strategiile de supraveghere, și de înțelegere a când, pentru a evita o intervenție., Îmbunătățirea datelor epidemiologice privind istoria naturală a febrei aftoase, asocierea cu evenimente cardiovasculare (de exemplu, accident vascular cerebral, disecția și anevrismul), și factori de risc sunt necesare și va fi esențial pentru a înțelege moleculară fiziopatologia febrei aftoase și comune și distincte de biologie în relație cu alte nonatherosclerotic arteriopathies. Înțelegerea geneticii FMD prin cercetarea PHACTR1 și a contribuitorilor genetici suplimentari la riscul FMD va sprijini ambele obiective., Aceste priorități necesită investigații în studii de cohortă, studii bazate pe familie, investigații genomice și de altă natură și stabilirea de biobanks de sânge, plasmă și țesut vascular.
a.
1. Olin JW, Gornik HL, Bacharach JM și colab. Displazia fibromusculară: starea științei și întrebările critice fără răspuns: o declarație științifică a American Heart Association. Circulație. 2014;129(9):1048-1078.
2. Palubinskas AJ, Ripley HR. Fibromuscular hiperplazie în extrarenal artere. Radiologie. 1964;82:451-455.
3., Olin JW, Froehlich J, Gu X și colab. Registrul Statelor Unite pentru displazia fibromusculară: rezultate la primii 447 de pacienți. Circulație. 2012;125(25):3182-3190.
4. Touze E, Oppenheim C, Trystram D, și colab. Displazia fibromusculară a arterelor cervicale și intracraniene. Int J Accident Vascular Cerebral. 2010;5(4):296-305.
5. Southerland AM, Meschia JF, Worrall BB. Comună a asociațiilor de nonatherosclerotic, mare, navă, cerebrovasculare arteriopathies: având în anevrismele intracraniene, disecție de arteră cervicală, boala moyamoya și displazia fibromuscular. Curr Opin Neurol. 2013;26(1):13-28.,
6. Stanley JC, Gewertz BL, Bove el, Sottiurai V, Fry WJ. Fibrodisplazia arterială. Caracterul histopatologic și conceptele etiologice actuale. Arch Surg. 1975; 110 (5):561-566.
7. Kiando SR, Tucker NR, Castro-Vega LJ, și colab. PHACTR1 este un locus de susceptibilitate genetică pentru displazia fibromusculară care susține modelul său genetic complex de moștenire. Te Rog, Genet. 2016; 12: e1006367.
8. Di Monaco S, Georges A, Lengele JP, Vikkula M, Persu A. genomica displaziei fibromusculare. Int J Mol Sci. 2018; 19 (5):pii:E1526.
9. Gupta RM, Hadaya J, Trehan A, și colab., O variantă genetică asociată cu cinci boli vasculare este un regulator distal al expresiei genei endotelinei-1. Celula. 2017; 170 (3): 522-533,e15.
10. Touze E, Southerland AM, Boulanger M, și colab. Displazia fibromusculară și manifestările sale neurologice: o revizuire sistematică. JAMA Neurol. 2019;76(2):217-226.
11. Kadian-Dodov D, Gornik HL, Gu X și colab. Disecția și anevrismul la pacienții cu displazie fibromusculară: constatări din registrul american pentru FMD. Sunt Coll Cardiol. 2016;68(2):176-185.
12. Mettinger KL, Ericson K. displazia fibromusculară și creierul. Eu., Observații privind caracteristicile angiografice, clinice și genetice. Accident vascular cerebral. 1982;13:46-52.
13. O ‘ Connor SC, Poria N, Gornik HL. Displazia fibromusculară: o actualizare pentru clinicianul durerii de cap. Dureri de cap. 2015;55(5):748-755.
14. Debette S, Leys D. disecțiile arterei cervicale: factori predispozanți, diagnostic și rezultat. Lancet Neurol. 2009;8(7):668-678.
15. Giroud M, Fayolle H, Andre N, și colab. Incidența disecției arterei carotide interne în comunitatea din Dijon. J Neurol Neurochirurgie Psihiatrie. 1994;57(11):1443.
16. Lee VH, Brown RD, Jr., Mandrekar JN, Mokri B., Incidența și rezultatul disecției arterei cervicale: un studiu bazat pe populație. Neurologie. 2006;67(10):1809-1812.
17. Bejot Y, Aboa-Eboule C, Debette S, și colab. Caracteristicile și rezultatele pacienților cu disecție multiplă a arterei cervicale. Accident vascular cerebral. 2014;45(1):37-41.
18. Cloft HJ, Kallmes DF, Kallmes MH, Goldstein JH, Jensen MINE, Dion JE. Prevalența anevrismelor cerebrale la pacienții cu displazie fibromusculară: o reevaluare. Neurochirurgul. 1998;88(3):436-440.
19. Lather HD, Gornik HL, Olin JW, și colab., Prevalența anevrismului intracranian la femeile cu displazie fibromusculară: un raport al Registrului american pentru displazia fibromusculară. JAMA Neurol. 2017;74(9):1081-1107.
20. Favoni V, Giani L, al-Hassany L, și colab. CGRP și migrenă din punct de vedere cardiovascular: ce ne așteptăm de la blocarea CGRP? J Durere De Cap. 2019;20(1):27.
21. Schievink WI, Mokri B, O ‘ Fallon WM. Disecție spontană recurentă a arterei cervicale. În Engl J Med. 1994;330(6):393-397.
22. Kennedy F, Lanfranconi S, Hicks C, și colab., Antiagregante plachetare vs anticoagulare pentru disecție: CADISS braț nonrandomized și meta-analiză. Neurologie. 2012;79(7):686-689.
23. Debette S. fiziopatologia și factorii de risc ai disecției arterei cervicale: ce am învățat de la cohortele mari din spital? Curr Opin Neurol. 2014;27(1):20-28.
24. Investigatori CADISS proces, Markus HS, Hayter E, și colab. Tratamentul antiplachetar comparativ cu tratamentul anticoagulant pentru disecția arterei cervicale (CADISS): un studiu randomizat. Lance. Neurol 2015; 14 (4):361-367.
25. Peng J, Liu Z, Luo C, și colab., Tratamentul disecției arterei cervicale: antitrombotice, tromboliză și terapie endovasculară. Biomed Res Int. 2017;2017:3072098.
26. Powers WJ, Rabinstein AA, Ackerson T, și colab. Ghid pentru managementul precoce al pacienților cu accident vascular cerebral ischemic acut: actualizare 2019 la orientările din 2018 pentru managementul timpuriu al AVC ischemic acut: un ghid pentru profesioniștii din domeniul sănătății de la American Heart Association/American Stroke Association. Accident vascular cerebral. 2019; 50 (12): e344-e418.
27. Kernan WN, Ovbiagele B, negru HR, și colab., Linii directoare pentru prevenirea accidentului vascular cerebral la pacienții cu accident vascular cerebral și atac ischemic tranzitoriu: un ghid pentru profesioniștii din domeniul sănătății de la American Heart Association/American Stroke Association. Accident vascular cerebral. 2014;45(7):2160-2236.
28. Debette S, Metso T, Pezzini A și colab. Asocierea factorilor de risc vascular cu disecția arterei cervicale și AVC ischemic la adulții tineri. Circulație. 2011;123(14):1537-1544.
29. Gornik HL, Persu A, Adlam D și colab. Primul consens internațional privind diagnosticul și managementul displaziei fibromusculare. Vasc Med. 2019;24(2):164-189.,
AMS primește sprijin de cercetare de la NIH (NINDS, NHLBI), AHA/ASA, Fondul de cercetare translațională Coulter și Diffusion Pharmaceuticals, Inc. De asemenea, ofer consultanță juridică de specialitate în cazurile de Neurologie vasculară.
BBW este un redactor-șef adjunct al revistei de Neurologie, primește finanțare de la NIH (curent NINDS,NCATS și înainte NINDS, NHGRI) și Australian-Americană Fulbright commission, și rapoarte nu suport comercial.




