de ce se extinde apa când îngheață?De ce apa lichidă are o densitate maximă?
majoritatea lichidelor au un comportament destul de simplu atunci când suntrăcit (la o presiune fixă): se micșorează.Lichidul se contractă pe măsură ce este răcit; deoarece moleculele se mișcă mai lent, ele sunt mai puțin capabile să depășească forțele atractiveintermoleculare care le apropie una de cealaltă.Apoi se atinge temperatura de îngheț și substanța se solidifică, ceea ce o face să se contracte mai mult, deoarece solidele cristaline sunt de obicei bine ambalate.,apa este una dintre puținele excepții de la acest comportament.Când apa lichidă este răcită, se contractă așa cum s-ar așteptapână la atingerea unei temperaturi de aproximativ 4 grade Celsius.După aceea, se extinde ușor până când ajunge la punctul de îngheț, iar atunci când îngheață, se extinde cu aproximativ 9%.acest comportament neobișnuit își are originea în structura filigranului.Există o puternică tendință de a forma o rețea de hydrogenbonds, în cazul în care fiecare atom de hidrogen este într-o linie între două oxygenatoms., Această tendință de legare a hidrogenului devine mai puternică pe măsură ce temperaturadevine mai mică (deoarece există mai puțină energie termică pentru a scutura hidrogenurile din poziție). Structura de gheață este complet hidrogen legați, și aceste obligațiuni vigoare structura cristalină a fi foarte „open”, după cum se arată în imaginea de mai jos: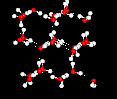
pozele De pe aceasta pagina sunt furnizate de curtoazie theMathMol proiect la NYU/ACF Vizualizare Științifice de Laborator.
informații despre MathMol pot fi găsite aici.,în următoarele două imagini, prima aratăo structură tipică a apei lichide, în timp ce a doua este o structură de gheață; rețineți spațiul suplimentar deschis în gheață.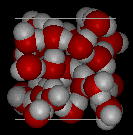
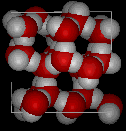
Acesta este deschis structură solidă, care cauzează de gheață să fie mai puțin densethan apă lichidă. De aceea, gheața plutește pe apă, pentru care ar trebui să fim cu toții recunoscători, deoarece dacă apa s-ar comporta „normal”, multe corpuri de apă ar îngheța solid în timpul iernii, ucigând toată viața din ele.”densitatea maximă” a apei este un produs al aceluiași fenomen.,Aproape de punctul de îngheț, moleculele de apă încep să se aranjezelocal în structuri asemănătoare gheții. Acest lucru creează o anumită „deschidere”în apa lichidă, care tinde să-și scadă densitatea.Acest lucru se opune tendinței normale de răcire de a creștedensitatea; este la aproximativ 4 grade Celsius că aceste tendințe opuse sunt echilibrate, producând densitatea maximă.
actualizat la 3 decembrie 2013




