Perché l’acqua si espande quando si congela?Perché l’acqua liquida ha una densità massima?
La maggior parte dei liquidi ha un comportamento abbastanza semplice quando vengono raffreddati (a una pressione fissa): si restringono.Il liquido si contrae man mano che viene raffreddato; poiché le molecole si muovono più lentamente, sono meno in grado di superare le forze intertermolecolari attraenti avvicinandole l’una all’altra.Quindi viene raggiunta la temperatura di congelamento e la sostanza si solidifica,il che fa sì che si contragga un po ‘ più perché i solidi cristallini sono solitamente ben imballati.,
L’acqua è una delle poche eccezioni a questo comportamento.Quando l’acqua liquida viene raffreddata, si contrae come se ci si aspettasse fino a raggiungere una temperatura di circa 4 gradi Celsius.Successivamente, si espande leggermente fino a raggiungere il punto di congelamento, quindi quando si blocca si espande di circa il 9%.
Questo comportamento insolito ha la sua origine nella struttura della filigrana.C’è una forte tendenza a formare una rete di idrogenobond, dove ogni atomo di idrogeno si trova in una linea tra due ossigenatomi., Questa tendenza legame idrogeno diventa più forte come la temperaturegets più basso (perché c’è meno energia termica per scuotere i hydrogenbonds fuori posizione). La struttura del ghiaccio è completamente legata all’idrogeno, e questi legami costringono la struttura cristallina ad essere molto “aperta”, come mostrato nella seguente immagine: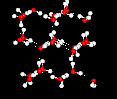
Le immagini in questa pagina sono fornite per gentile concessione del progetto Mathmol presso il Laboratorio di visualizzazione scientifica NYU/ACF.
Informazioni su MathMol possono essere trovate qui.,
Nelle due immagini seguenti, la prima mostrauna struttura tipica dell’acqua liquida, mentre la seconda è una struttura anice; nota lo spazio aperto extra nel ghiaccio.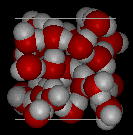
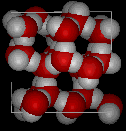
È questa struttura solida aperta che fa sì che il ghiaccio sia meno denso dell’acqua liquida. Questo è il motivo per cui il ghiaccio galleggia sull’acqua, per il quale dovremmo essere tutti grati perché se l’acqua si comportasse “normalmente” molti corpi d’acqua congelerebbero solidi in inverno, uccidendo tutta la vita al loro interno.
La “densità massima” dell’acqua è un prodotto dello stesso fenomeno.,Vicino al punto di congelamento, le molecole d’acqua iniziano a organizzarsilocalmente in strutture simili a ghiaccio. Questo crea una certa “apertura” nell’acqua liquida, che tende a diminuire la sua densità.Ciò si oppone alla normale tendenza del raffreddamento ad aumentare la densità; è a circa 4 gradi Celsius che queste tendenze opposte sono bilanciate, producendo la densità massima.
Aggiornato il 3 dicembre 2013




