Un ligando è uno ion o una molecola che si lega a un atomo metallico centrale per formare un complesso (alternativamente noto come entità di coordinazione).

I ligandi sono generalmente considerati come donatori di elettroni attratti dal metallo al centro del complesso. I metalli sono accettori di elettroni.
I ligandi possono essere specie neutre o caricate negativamente con coppie di elettroni disponibili. L’acqua è un ligando comune., Qui viene mostrata una molecola d’acqua con le sue due coppie solitarie di elettroni.

Una coppia di elettroni dal ligando, come l’acqua, fornisce entrambi gli elettroni per il legame che si forma tra se stesso e l’atomo o lo ion metallico centrale.
Qui un singolo ligando L, che potrebbe essere acqua, dona una coppia di elettroni per formare un legame con un atomo di metallo M.
Ligandi monodentati
I ligandi monodentati hanno un solo atomo in grado di legarsi a un atomo o ion metallico centrale.
H20 e NH3 sono esempi di ligandi monodentati neutri.,
Quando H20 è un ligando, l’ossigeno è l’atomo donatore che si lega al metallo. Quando NH3 è un ligando, l’azoto è l’atomo donatore che si lega al metallo.
Esempi di ligandi monodentati caricati elettricamente sono ioni alogenuri, come: F -, Cl -, Br -, I-e ciano, CN-.
La carica complessiva su un complesso è la somma aritmetica dello stato di ossidazione del metallo al centro più la carica(s) portata al complesso da ciascun ligando.
Ligandi polidentati
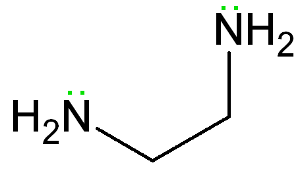 Esempio di ligando bidentato., L’etano-1,2-diammina ha due coppie solitarie di elettroni mostrate in verde.
Esempio di ligando bidentato., L’etano-1,2-diammina ha due coppie solitarie di elettroni mostrate in verde.Una molecola di ligando con più di un atomo donatore è un ligando chiamato polidentato. Questi sono dati nomi specifici, a seconda di quanti atomi donatori contengono.
I ligandi bidentati
I ligandi bidentati hanno due atomi in grado di legarsi a un atomo o uno ion metallico centrale.
Etano-1,2-diammina (mostrato nell’immagine) è un esempio di un ligando bidentato.
Entrambi i nitrogeni in questa molecola possono agire come donatori di elettroni, legandosi con un atomo o uno ion metallico centrale.,
Altri esempi di ligandi bidentati sono lo acetyl acetilacetonato, noto come (acac), e lo ion ossalato (ox).
 Esempio di ligando tridentato. 1,4,7-triazaheptane (noto anche come dietilenetriamina) ha tre coppie solitarie di elettroni mostrate in verde.
Esempio di ligando tridentato. 1,4,7-triazaheptane (noto anche come dietilenetriamina) ha tre coppie solitarie di elettroni mostrate in verde.I ligandi Tridentati e i ligandi polidentati superiori
I ligandi Tridentati hanno tre atomi in grado di legarsi a un atomo o uno ion metallico centrale.,
Le molecole con quattro atomi donatori sono chiamate ligandi tetradentati; cinque atomi donatori, pentadentati; e sei atomi donatori esadentati.
Un complesso che contiene un ligando polidentato è chiamato chelato.
L’immagine mostrata sotto del legame di EDTA ad un atomo metallico centrale è un esempio di un chelato. Inoltre, vedi composti della corona.
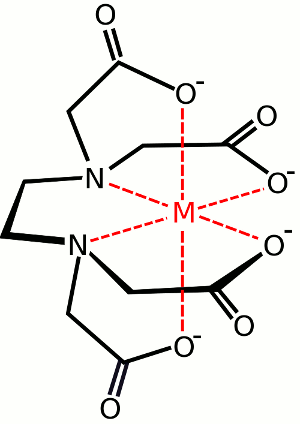 Esempio di ligando esadentato. EDTA (noto anche come acido etilendiamminotetraacetico). L’immagine mostra un complesso formato tra EDTA e una specie metallica centrale.,Se il metallo fosse Fe in stato di ossidazione III, il complesso sarebbe-
Esempio di ligando esadentato. EDTA (noto anche come acido etilendiamminotetraacetico). L’immagine mostra un complesso formato tra EDTA e una specie metallica centrale.,Se il metallo fosse Fe in stato di ossidazione III, il complesso sarebbe- Ligandi ambidentati
I ligandi ambidentati sono ligandi monodentati che possono legarsi in due punti possibili. Ad esempio, lo nitrate nitrato NO2 – può legarsi all’atomo/ion metallico centrale all’atomo di azoto o ad uno degli atomi di ossigeno.Lo thi tiocianato, SCN-può legarsi al metallo centrale allo zolfo o all’azoto.




