INTRODUCTION
la progression de la CKD implique l’initiation de multiples mécanismes régulateurs compensateurs, tels que la stimulation de la glande parathyroïde avec augmentation conséquente des niveaux circulants de PTH. Pendant des années, une série de facteurs ont été identifiés dans le développement de l’hyperparathyroïdie secondaire, qui pourrait également être responsable de l’augmentation de la morbidité et de la mortalité observée chez les patients dialysés.,1-3
La régulation des niveaux de PTH est contrôlée par un mécanisme de rétroaction complexe, dans lequel les niveaux de calcium ionique,4 calcitriol5 ou ses dérivés6,7 et de faibles niveaux de phosphorus8 inhibent la sécrétion de PTH. D’autres facteurs ont également été décrits, qui peuvent agir sur la glande parathyroïde modifiant la sécrétion et/ou la synthèse de la PTH, tels que l’aluminium,9 œstrogènes,10 magnésium, les corticostéroïdes et certaines cytokines.11 plus récemment, le facteur de croissance des fibroblastes 23 (FGF-23) a été ajouté à cette liste, qui est capable d’inhiber directement la synthèse et la sécrétion de PTH.,12
la glande parathyroïde est régulée par ses récepteurs, parmi lesquels se distinguent le CaR, le VDR et le récepteur du facteur de croissance des fibroblastes (FGFR). Bien que de nombreux processus de régulation soient spécifiquement médiés par ces récepteurs, leur rôle et leurs mécanismes de signalisation sont controversés., Les effets du calcium, du calcitriol et même du phosphore sur la fonction parathyroïdienne ont lieu par des mécanismes spécifiques; cependant, il existe également des actions indirectes qui dépendent de la connexion et de l’interrelation étroites entre le calcium, le calcitriol et le phosphore sur les récepteurs du calcium et de la vitamine D impliqués dans la régulation parathyroïdienne. Dans cet article, nous avons l’intention de réviser et de mettre à jour de manière critique le rôle des récepteurs CaR et VDR dans la production de PTH.
calcium et récepteur du CALCIUM
L’ion calcium extracellulaire est le principal régulateur parathyroïdien.,13 de faibles niveaux de calcium stimulent la sécrétion de PTH en quelques minutes, tandis que des niveaux élevés inhibent la libération d’hormones et favorisent la dégradation dans les cellules parathyroïdes elles-mêmes.14 Il en résulte une réponse sigmoïdale de la glande parathyroïdienne, dans laquelle de petits changements de l’ion calcium extracellulaire provoquent de grandes variations de PTH, acquérant sa plus grande inhibition dans l’hypercalcémie.
Les effets du calcium sur la PTH sont médiés par son récepteur spécifique, CaR,15 qui appartient à la famille des récepteurs couplés aux protéines G, il est présent sur la membrane des cellules parathyroïdes., Une augmentation du calcium extracellulaire est détectée par CaR, ce qui déclenche une cascade de signalisation intracellulaire qui entraîne l’inhibition de la sécrétion et de la synthèse de la PTH.
bien que l’expression de La CaR, tout comme son ARN messager (ARNm) et son produit protéique, puisse être modifiée dans de nombreuses circonstances. Dans la majorité des cas, les raisons pour lesquelles cela se produit n’ont pas été clarifiées. Diverses études ont observé une diminution spectaculaire de L’expression de CaR dans des cultures de cellules parathyroïdes monocouches ou dispersées,16,17, mais pas lorsque les glandes sont cultivées de manière entière, fragmentée ou laminée.,18 compte tenu de ces résultats, et bien que le mécanisme sous-jacent soit inconnu, il semble que L’expression de La CaR dépend de la structure tridimensionnelle du tissu. En effet, lorsque les cellules parathyroïdes dispersées sont cultivées dans une matrice de collagène qui permet leur regroupement sous une forme ressemblant au tissu parathyroïdien (pseudogland), l’expression du récepteur se rétablit.19
en outre, bien que l’action principale de la CaR soit de détecter le calcium, l’expression et la concentration de La CaR dans les glandes parathyroïdes ne semblent pas dépendre des niveaux extracellulaires de calcium., Des études in vivo ont montré que les animaux nourris avec un régime riche ou faible en calcium ne montrent pas de différences dans les niveaux de CaR dans les glandes parathyroïdes, suggérant que le calcium n’a pas d’effet régulateur sur son récepteur.20,21 néanmoins, lors de l’interprétation et de l’analyse des résultats, il est fondamental de tenir compte du fait que dans les études in vivo, les variations de l’un des facteurs régulant la PTH peuvent également induire des changements dans d’autres facteurs également capables de réguler la PTH, dissimulant ou perturbant ainsi le véritable effet du facteur étudié., Dans une étude récente de notre groupe22, nous avons essayé de répondre à ces questions en ne modifiant qu’un seul des régulateurs et en maintenant le reste constant. Ainsi, nous avons démontré dans les glandes parathyroïdes de rats normaux que l’augmentation des concentrations de calcium abaissait les niveaux de mRNAlevels de PTH, mais pas l’expression de CaR, indiquant que cet effet était dû à l’activation du récepteur mais pas à l’augmentation de ses niveaux., Au cours des 24 heures de culture avec les différentes concentrations de calcium, les niveaux D’ARNm CaR et de protéines n’ont pas changé même en doublant la concentration de calcium présent dans le milieu de culture (figure 1).
récepteur du CALCITRIOL et de la vitamine D
le Calcitriol est également un régulateur important de la glande parathyroïde et exerce un effet direct sur la sécrétion de PTH en inhibant la synthèse de son ARNm.14
le Calcitriol agit sur la glande parathyroïde à travers son récepteur spécifique, le VDR, un récepteur à haute affinité et spécificité, qui appartient au groupe des récepteurs stéroïdiens / thyroïdiens., Lorsque le calcitriol se lie à son récepteur, il produit la translocation du complexe calcitriol – VDR au noyau cellulaire, formant un hétérodimère avec le récepteur x rétinoïde (RXR). Le complexe Calcitriol-VDR-RXR lie les éléments sensibles à la vitamine D (VDRE) présents dans la région du promoteur du gène PTH, bloquant sa transcription. De plus, le calcitriol est capable d’inhiber indirectement la sécrétion de PTH en augmentant l’absorption du calcium dans l’intestin, tout en stimulant la résorption osseuse et l’élimination du calcium.,23
contrairement à ce qui se produit avec le calcium et la CaR, le calcitriol régule l’expression de son propre récepteur (VDR), stimulant sa synthétise24 et augmentant sa durée de vie moyenne.25 par conséquent, le déficit en calcitriol observé chez les patients atteints d’IRC est associé à une diminution des taux de VDR dans la glande parathyroïdienne.,26 Jusqu’à présent, toutes les études sur l’effet du calcitriol sur les taux de VDR ont toujours été réalisées in vivo,27-29 et il a été observé que la régulation du VDR par le calcitriol n’avait été efficace que dans des conditions hypercalcémiques et normocalcémiques, et non dans l’hypocalcémie, ce qui suggère que les taux de calcium peuvent être critiques pour contrôler les taux de VDR., Cependant, dans une étude récente22 dans laquelle les glandes parathyroïdes ont été cultivées dans de faibles niveaux de calcium, nous avons observé que le calcitriol était capable d’augmenter les niveaux d’ARNm VDR et de protéines (figure 2), suggérant une moindre dépendance VDR en relation avec la concentration en calcium.
coopération entre le CALCIUM, le CALCITRIOL, le CaR et le VDR
outre l’effet décrit du calcium et du calcitriol sur ses propres récepteurs, les deux peuvent coopérer en modifiant la réponse de l’autre de manière positive., Même si le VDR est le récepteur spécifique du calcitriol et d’autres métabolites analogues de la vitamine D, le calcium est également capable de réguler les niveaux de VDR. Divers dans vivo28, 29 et dans vitro22,29 des études ont décrit cet effet, comme l’étude récemment mentionnée par notre groupe22 dans laquelle il a été observé qu’après 24 heures de culture des glandes parathyroïdes avec du calcium, les niveaux d’ARNm VDR et de protéines (figure 3a y 3B) augmentaient.
Il a également été décrit que le calcitriol peut également réguler la CaR, bien que dans ce cas les résultats soient encore contradictoires., Certaines études n’ont pas détecté de variations dans les niveaux de CaR avec le calcitriol.21 D’autres ne constatent une augmentation de la CaR que dans des conditions normales et hypercalcémiques,20,29 tandis que d’autres chercheurs ont observé cet effet même lorsque les glandes parathyroïdes sont cultivées avec une faible concentration de calcium.22 dans ces conditions, il a été démontré que le calcitriol, après 48 heures de culture, augmente non seulement l’ARNm CaR mais aussi sa protéine (figure 3c y 3D). On a émis l’hypothèse que cet effet du calcitriol sur le CaR pourrait être médié par le VDRE, également présent dans le promoteur du gène CaR.,30
autres facteurs modulaires du CaR et du VDR
en plus de la régulation que le calcium et le calcitriol exercent sur leurs récepteurs, il existe d’autres facteurs et médicaments qui peuvent réguler les niveaux de CaR et de VDR. L’un de ces facteurs est le phosphore, qui en plus d’exercer une régulation directe de la PTH en augmentant sa sécrétion,31 Il peut exercer une régulation indirecte, modifiant L’expression de la CaR et de la VDR, bien que ce sujet soit débattu., Dans le cas de La CaR, certaines études ont montré qu’un régime riche en phosphore est capable de réduire l’expression de la Car32-34,bien que des travaux in vivo antérieurs n’aient pas détecté de changements dans l’expression de La CaR dans les glandes parathyroïdes avec des régimes riches ou faibles en phosphore.35,36
de plus, certains chercheurs ont démontré que le phosphore pouvait modifier l’expression du VDR. Cet effet semble être spécifique aux tissus, étant donné que dans l’intestin, le phosphore pourrait augmenter L’expression du VDR alors qu’il pourrait l’abaisser dans le rein.37 Il est important de souligner ici le rôle des liants phosphatés., L’hyperphosphatémie caractéristique des stades avancés de L’IRC pourrait être responsable des variations des taux de CaR et de VDR dans les glandes parathyroïdes. L’utilisation de liants phosphatés pour réduire l’hyperphosphatémie pourrait aider à normaliser les niveaux d’expression de la CaR et de la VDR.
L’Aluminium est un autre facteur capable de réguler la fonction parathyroïdienne en inhibant la sécrétion de PTH qui pourrait intervenir dans la régulation CaR et VDR.,38 des études antérieures de notre groupe ont démontré l’existence d’un effet inhibiteur dépendant de la dose d’aluminium sur les taux D’ARNm de la PTH chez des rats atteints d’insuffisance rénale chronique39,en réduisant l’expression du gène CaR par un mécanisme posttranscriptionnel.9 toutefois, on ne sait pas si l’aluminium a un effet sur le VDR.
enfin, les calcimimétiques, qui modulent la CaR allostériquement, augmentent la sensibilité du récepteur au calcium extracellulaire et réduisent la sécrétion de PTH.40-42 ils semblent également avoir un effet sur VDR en augmentant son expression et en réduisant la synthèse de PTH43.,
En résumé, les mécanismes de régulation de la PTH sont complexes. Plusieurs facteurs sont impliqués dans cette régulation et exercent leurs actions à travers des récepteurs spécifiques par des mécanismes directs et indirects qui modulent l’expression de ces récepteurs, ce qui modifie en même temps le niveau de réponse des glandes parathyroïdes.
Remerciements
Cette étude a été soutenue par le Fondo de Investigaciones Sanitarias (FIS 02/0688) (ISCIII-Retic-RD06, REDinREN, (16/06) et la Fundación Renal Íñigo Álvarez de Toledo., Au cours du développement de ce projet, Natalia Carrillo-López a reçu une subvention de la Fondation rénale Íñigo Álvarez de Toledo, et plus tard un contrat de recherche de REDinREN (ISCIIIRetic-RD06, REDinREN 16/06) Pablo Román-García et Dr.Daniel Álvarez-Hernández, Dr. Ignacio González-Suárez et Dr. ManuelNaves-Díaz ont également contribué au développement du projet.
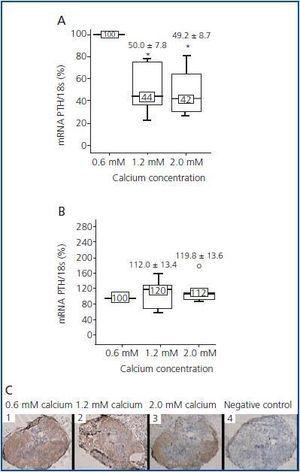
la Figure 1.

la Figure 2.,
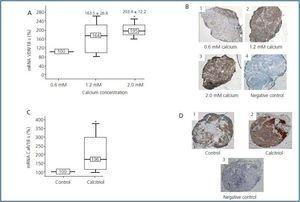
la Figure 3.




