Pourquoi l’eau élargir quand il gèle?Pourquoi l’eau liquide ayant une densité maximale?
la plupart des liquides ont un comportement assez simple lorsqu’ils sont refroidis (à une pression fixe): ils rétrécissent.Le liquide se contracte à mesure qu’il est refroidi; parce que les molécules se déplacent plus lentement, elles sont moins capables de surmonter les forces inter-moléculaires attrayantes les rapprochant les unes des autres.Ensuite,la température de congélation est atteinte et la substance se solidifie, ce qui la fait se contracter davantage parce que les solides cristallins sont généralement bien emballés.,
l’Eau est l’une des rares exceptions à ce comportement.Lorsque l’eau liquide est refroidie, elle se contracte comme on s’y attendrait jusqu’à ce qu’une température d’environ 4 degrés Celsius soit atteinte.Après cela, il se dilate légèrement jusqu’à ce qu’il atteigne le point de congélation, puis quand il gèle, il se dilate d’environ 9%.
ce comportement inhabituel trouve son origine dans la structure de la watermolécule.Il y a une forte tendance à former un réseau d’hydrogenbonds, où chaque atome d’hydrogène est dans une ligne entre deux oxygénatomes., Cette tendance à la liaison hydrogène devient plus forte à mesure que la température diminue (car il y a moins d’énergie thermique pour secouer les hydrogénobonds hors de position). La structure de la glace est complètement liée à l’hydrogène, et ces liaisons forcent la structure cristalline à être très « ouverte », comme le montre l’image suivante: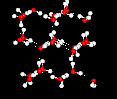
Les images de cette page sont fournies avec l’aimable autorisation du projet theMathMol au Laboratoire de visualisation scientifique NYU/ACF.
des informations sur MathMol peuvent être trouvées ici.,
dans les deux images suivantes, la première montre une structure typique de l’eau liquide, tandis que la seconde est une structure anice; notez l’Espace ouvert supplémentaire dans la glace.
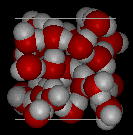
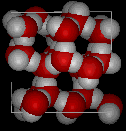
c’est cette structure solide ouverte qui fait que la glace est moins dense que l’eau liquide. C’est pourquoi la glace flotte sur l’eau, pour laquelle nousdevrait tous être reconnaissants parce que si l’eau se comportait « normalement » de nombreux plans d’eau gèleraient solides en hiver, tuant toute la vie en eux.
la « densité maximale » de L’eau est le produit du même phénomène.,Près du point de congélation, les molécules d’eau commencent à s’arrangerlocalement dans des structures ressemblant à de la glace. Cela crée une certaine « ouverture » dans l’eau liquide, ce qui tend à diminuer sa densité.À cela s’oppose la tendance normale du refroidissement à augmenter la densité; c’est à environ 4 degrés Celsius que ces tendances opposées sont équilibrées, produisant le maximum de densité.
Mise à jour le 3 décembre 2013




